Влияние
различных факторов на производительность процесса.
а) Влияние параметров процесса на удельную
производительность реакторов.
Влияние начальных концентраций и давлений на производительность определяется
видом кинетических уравнений. Так, для необратимых реакций, описываемых кинетическими
уравнениями простого типа
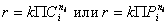
последние можно
преобразовать в выражения
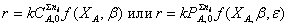
где e -
коэффициент изменения объема в газофазных реакциях, b - начальное соотношение
реагентов.
При подстановке этих выражений в уравнения производительности в конечном
выражении последние для любого реактора множители 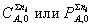 останутся. Например,
останутся. Например, 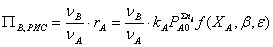 .
.
Из этого следует, что удельная производительность реакторов для реакций,
описываемых кинетическими уравнениями простого типа при прочих равных условиях,
будет прямо пропорциональна начальным концентрациям или парциальным давлениям в
степени, равной суммарному порядку реакции.
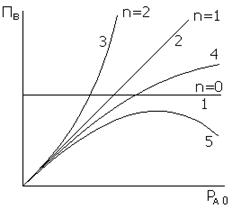 Такие
зависимости представлены на рисунке для реакций нулевого, первого и второго
порядков. Для реакций с кинетическим уравнением
Такие
зависимости представлены на рисунке для реакций нулевого, первого и второго
порядков. Для реакций с кинетическим уравнением
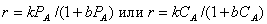
удельная
производительность растет по затухающей кривой (4). Для зависимости
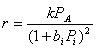
кривая при
определенных значениях Ха и bi может проходить через
максимум (5).
Пример 1.
Найти общее решение максимальной удельной производительности реактора идеального
смешения для реакции с кинетическим уравнением
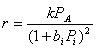
Решение.
Для простой необратимой реакции имеем

Для нахождения условий максимума берем производную и приравниваем ее к нулю:
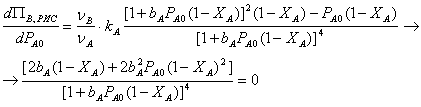
Выражение может равняться нулю при условии, что
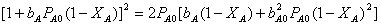
Дальнейшие преобразования и решение квадратного уравнения дают
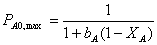
Следовательно, максимум удельной производительности достигается при тем
меньшем парциальном давлении реагента, чем выше его адсорбционный коэффициент и
ниже степень конверсии реагентов.
Аналогичная ситуация имеет место для обратимых реакций
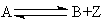
В этом случае кинетическое уравнение будет определяться зависимостью
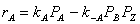
Парциальные давления компонентов могут быть выражены следующими равенствами
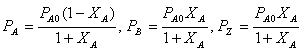
Тогда уравнение скорости приобретает вид
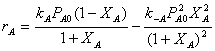
Производительность по продукту В для реактора идеального смешения
выразится как
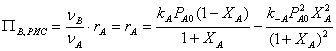
Максимальной производительности реактора соответствует условие
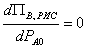
откуда следует
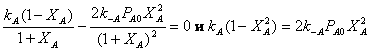
Тогда 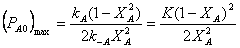
В то же время для обратимых реакций
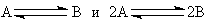
парциальное
давление реагента будет оказывать ускоряющее действие на процесс, степень
которого снижается с приближением конверсии к равновесной величине.
С другой стороны, для обратимых реакций типа
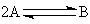
давление будет
выступать одновременно и фактором скорости и фактором смещения равновесия в
сторону продуктов.
Еще один способ воздействия на удельную производительность реакторов
состоит в применении избытка одного из реагентов, если оба они влияют на скорость
реакции. Так, для реакции 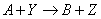 с кинетическим уравнением
с кинетическим уравнением
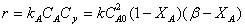
получим удельную
производительность реактора полного смешения
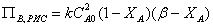
Можно видеть, что применяя избыток второго реагента Y, можно при той же конверсии повысить
удельную производительность или при постоянстве последней увеличить степень
конверсии, а следовательно, сделать сделать более экономичным рецикл.
Прием введения избытка более дешевого реагента широко используется в
химической технологии (гидролиз хлорпроизводных и алкилсульфатов, гидрирование
органических соединений водородом, контактное окисление SO2 в SO3 в присутствии серной кислоты).
Для обратимых реакций этот эффект дополняется смещением равновесия с возможностью
более полного превращения основного реагента в продукты.
В связи с изложенным следует отметить, что для газофазных реакций с
фиксированным общим давлением и кинетическим уравнением типа
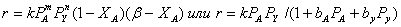 и др.
и др.
удельная
производительность реакторов всегда имеет максимум при определенном соотношении
реагентов.
Пример.
Определите соотношения реагентов в реакции 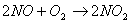 , осуществляемой при атмосферном давлении, которому
соответствует максимальная производительность, если скорость реакции
описывается уравнением
, осуществляемой при атмосферном давлении, которому
соответствует максимальная производительность, если скорость реакции
описывается уравнением 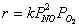 .
.
Решение.
Для реактора идеального смешения производительность по NO2 определяется соотношением
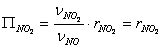
Обозначим количество молей исходного О2 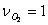 , а число молей NO=b.
Тогда суммарное количество молей равно 1+b.
, а число молей NO=b.
Тогда суммарное количество молей равно 1+b.
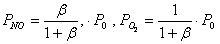
Тогда 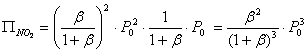
Оптимальному соотношению реагентов соответствует условие
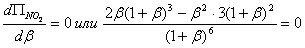
откуда следует 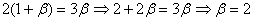 .
.
т.е. соотношение
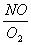 равно стехиометрическому. Можно ожидать, что это решение распространяется
на все газофазные реакции.
равно стехиометрическому. Можно ожидать, что это решение распространяется
на все газофазные реакции.
б) Влияние степени конверсии.
Большое влияние на удельную производительность реакторов оказывает
степень конверсии. Так, для простой необратимой реакции с кинетическим уравнением
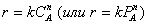 при проведении ее в
аппарате идеального смешения при
при проведении ее в
аппарате идеального смешения при 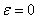 имеем
имеем 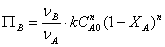 . Следовательно, с повышением степени конверсии удельная
производительность падает тем более резко, чем выше суммарный порядок (рисунок,
кривые 2 и 3), причем при
. Следовательно, с повышением степени конверсии удельная
производительность падает тем более резко, чем выше суммарный порядок (рисунок,
кривые 2 и 3), причем при 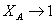 производительность
стремится к нулю. Для реакторов идеального вытеснения ее снижение с конверсией
выражено не так сильно (см. рисунок, кривые 1 и 2), вследствие чего эти
реакторы предпочтительны для процессов, где особенно желательна высокая степень
конверсии сырья.
производительность
стремится к нулю. Для реакторов идеального вытеснения ее снижение с конверсией
выражено не так сильно (см. рисунок, кривые 1 и 2), вследствие чего эти
реакторы предпочтительны для процессов, где особенно желательна высокая степень
конверсии сырья.
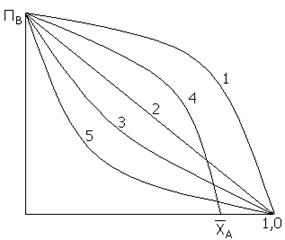 Рисунок.
Зависимость удельной производительности от степени конверсии для реакций
первого (2) и второго (3) порядков в РИС; для реакций первого (1) и второго (2)
в РИВ; для обратимой реакции (4); для реакций, тормозимых образующимися
продуктами (5).
Рисунок.
Зависимость удельной производительности от степени конверсии для реакций
первого (2) и второго (3) порядков в РИС; для реакций первого (1) и второго (2)
в РИВ; для обратимой реакции (4); для реакций, тормозимых образующимися
продуктами (5).
В случае обратимых реакций (кривая 4) удельная производительность
стремится к нулю, когда степень конверсии приближается к равновесной, а движущая
сила обратимой реакции 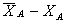 – к нулю. Для реакций,
которые тормозятся образующимися продуктами, удельная производительность падает
с повышением степени конверсии особенно сильно (кривая 5) (кинетическое уравнение
– к нулю. Для реакций,
которые тормозятся образующимися продуктами, удельная производительность падает
с повышением степени конверсии особенно сильно (кривая 5) (кинетическое уравнение
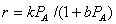 ).
).
Таким образом, для реакций, характеризующихся суммарным порядком 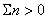 удельная производительность
существенно зависит от степени конверсии, падая до нуля при ХА=1 для
необратимых реакций
удельная производительность
существенно зависит от степени конверсии, падая до нуля при ХА=1 для
необратимых реакций 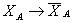 – для обратимых
реакций. Последнее показывает, что для полного завершения реакции требуется
бесконечно большой объем реактора, что практически невозможно. Это – одна из
причин широко распространенного в промышленности неполного превращения
реагентов, которые после разделения смеси возвращаются в процесс (рецикл
исходных реагентов).
– для обратимых
реакций. Последнее показывает, что для полного завершения реакции требуется
бесконечно большой объем реактора, что практически невозможно. Это – одна из
причин широко распространенного в промышленности неполного превращения
реагентов, которые после разделения смеси возвращаются в процесс (рецикл
исходных реагентов).
в) Влияние температуры.
В уравнение скорости реакции, и, соответственно производительности,
входит константа скорости, существенно зависящая от температуры. В подавляющем
большинстве случаев константа скорости сильно возрастает с ростом температуры.
Поэтому температура является важнейшим фактором производительности процессов.
Если в основе процессов лежат обратимые или необратимые эндотермические
реакции, то производительность процессов возрастает с ростом температуры во
всем мыслимом ее диапазоне. В случае обратимых эндотермических реакций
температура одновременно действует как фактор ускорения реакции и как фактор
смещения равновесия в сторону продуктов. Это хорошо иллюстрируется кинетическим
уравнением таких реакций, например, для реакции 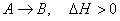
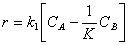 (1)
(1)
С ростом
температуры возрастает и константа скорости реакции 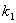 и константа равновесия
К. В результате растет сомножитель
и константа равновесия
К. В результате растет сомножитель 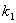 и сомножитель, заключенный
в квадратную скобку.
и сомножитель, заключенный
в квадратную скобку.
По иному обстоит дело у обратимых экзотермических реакций (DН>0), когда требования кинетики и
термодинамики взаимно противоположны. В этой случае с ростом температуры
возрастает член 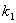 , но уменьшается константа равновесия К, что приводит уменьшению значения сомножителя, заключенного в
квадратные скобки. Противоборство этих двух факторов обусловливает
экстремальную зависимость производительности от температуры. Очевидно, что
положение температурного экстремума зависит от степени конверсии реагентов, так
как входящие в уравнение (1) концентрации компонентов зависят от глубины протекания
процесса
, но уменьшается константа равновесия К, что приводит уменьшению значения сомножителя, заключенного в
квадратные скобки. Противоборство этих двух факторов обусловливает
экстремальную зависимость производительности от температуры. Очевидно, что
положение температурного экстремума зависит от степени конверсии реагентов, так
как входящие в уравнение (1) концентрации компонентов зависят от глубины протекания
процесса
Оптимальная температура тем ниже, чем выше степень конверсии и для
данного случая выгодно постепенно понижающийся профиль температур (рис. )