Атомный спектральный анализ. Общая характеристика, аппаратурное оформление.
Эмиссионный спектральный анализ.
Теоретические основы эмиссионной спектроскопии.
Методы эмиссионного спектрального анализа основаны на измерении длины волны, интенсивности и других характеристик света, излучаемого атомами и ионами вещества в газообразном состоянии.
Испускание света атомами происходит за счет изменения энергии атомов. Атомы могут обладать только строго определенными дискретными запасами внутренней энергии: Е0 , Е1 , E2 и т. д. В невозбужденном, т. е. нормальном, состоянии атомы обладают минимальной энергией Е0 . При подведении энергии, например при столкновении с быстролетящими электронами, энергия которых достаточна для возбуждения, атомы возбуждаются, т. е. переходят на более высокий энергетический уровень: Е1 , E2 и т. д.
Через очень короткое время (~10-8 с) атом самопроизвольно
возвращается в нормальное или какое-то более низкое возбужденное состояние.
Освобождающаяся при этом энергия ![]() E
излучается в виде светового кванта hv:
E
излучается в виде светового кванта hv:
![]() E = hv
E = hv
Частота излучения n определяется соотношением
![]() (1)
(1)
где ЕA* и EA - энергия атома в возбужденном и нормальном состояниях.
Или, характеризуя излучение волновым числом (n ', см-1),
![]() (2)
(2)
где с — скорость света.
Эти величины получили название спектральных термов Т:
![]()
![]() (7)
(7)
Следовательно,
![]()
Термы атома водорода могут быть непосредственно вычислены по соотношениям (7). Приняв в (7), например, п1 = 1, получим T1(n1=1) = R/1 = 109678.76 см-1.
Если принять п1 = 2, а n* > 3, то получим частоты линий, образующих серию Бальмера; при п1 = 3 и n* > 4 - серию Паше на и т.д. С учетом заряда ядра z формула (6) принимает вид
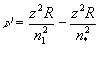 (8)
(8)
полный вывод системы термов для данной электронной конфигурации остается довольно трудоемким.
Терм основного состояния обычно определяют, пользуясь правилами Хунда:
1. Основное, т. е. низшее, энергетическое состояние имеет наибольшее значение суммарного спина (мультиплетности).
2. Среди термов с максимальной мультиплетностью низшим является тот, у которого
наибольшее значение L.
3. Низшим компонентом мультиплета будет J = L — S, если уровень заполнен меньше чем наполовину, и J = L + S, если он заполнен больше чем наполовину.
Наиболее яркой в спектре будет линия, отвечающая переходу с первого возбужденного уровня на основной. Линию, отвечающую этому переходу, называют резонансной. Например, у натрия резонансными являются переходы 2P3/2, - 2S1/2, и 2P1/2 — 2S1/2 , им отвечают линии с длиной волны 588,996 и 589,593 нм. Это излучение, в частности, окрашивает пламя горелки в желтый цвет при введении солей натрия.
Спектр атома любого элемента существенно отличается от спектра его иона в связи с изменением числа оптических электронов при ионизации. Поэтому в таблицах спектральных линий рядом с символом химического элемента приводят римскую цифру, по которой можно судить о кратности ионизации атома. Цифра I относится к нейтральному атому (например, Fe(I) относится к Fe), цифра II—к однократно ионизированному атому (например, Fe(II) относится к Fe+) и т. д.
Интенсивность спектральной линии Ikr приближенно определяется выражением
Ikr = NkrAkrhn kr (9)
где Nk — число атомов в возбужденном состоянии k ; Akr — вероятность перехода из возбужденного состояния k в более низкое состояние r; vkr — частота, соответствующая этому переходу; h — постоянная Планка.
Интенсивность спектральной линии зависит от температуры.
При постоянстве температуры и других условий возбуждения уравнение (11) переходит в
Если режим работы источника возбуждения достаточно стабилен и скорость подачи вещества в плазму постоянна, наступает некоторое стационарное состояние, при котором число атомов элемента в плазме оказывается пропорциональным концентрации этого элемента в пробе:
N=a "c, (13)
где с — концентрация вещества в пробе; a " — коэффициент пропорциональности.
Подставляя соотношения (12) и (13) в (11), получаем
Не все кванты, испускаемые возбужденными частицами, достигают приемника света. Квант света может быть поглощен невозбужденным атомом и, таким образом, не будет зафиксирован приемником излучения. Это так называемое самопоглощение. С увеличением концентрации вещества самопоглощение возрастает.
Самопоглощение учитывается в уравнении Ломакина:
I=acb (15)
где коэффициент а зависит от режима работы источника возбуждения, его стабильности, температуры и т.д.; b — коэффициент самопоглощения, учитывающий поглощение квантов света невозбужденными атомами.
При логарифмировании уравнения (15) получаем:
lgI=lga+b* lgc (16)
Линейная зависимость lgI от lgc очень удобна для построения градуировочного графика. Уравнение (16) является основой количественного спектрального анализа.
Важной характеристикой является ширина спектральной линии. Спектральная линия — это оптическое изображение щели спектрального прибора.Тем не менее, хотя все спектральные линии в данном спектре являются изображением одной и той же щели и, казалось бы, должны иметь одинаковую ширину, она на самом деле различна.
4. С увеличением концентрации элемента в пробе возрастает самопоглощение, что приводит к уменьшению интенсивности центральной части линии и ее уширению.
Очень широкие и очень узкие спектральные линии менее пригодны для спектрального анализа, чем линии средней ширины.
Основные узлы спектральных приборов.
Прибор для проведения спектрального анализа имеет следующие основные узлы: источник возбуждения, диспергирующий элемент и приемник света. Кроме этих основных узлов в любом спектральном приборе есть оптическая система, предназначенная для получения параллельного пучка света, его фокусировки, изменения хода лучей.
В источнике возбуждения вещество атомизируется и возбужденные атомы или ионы испускают свет, который диспергирующим элементом разделяется в пространстве на отдельные составляющие, а приемник света их фиксирует.
Источники возбуждения.
Источники возбуждения переводят пробу из конденсированной фазы в парообразную и возбуждают вещество в этой фазе. В большинстве источников возбуждения эти функции совмещаются, однако в некоторых случаях применяют два устройства: одно для получения газовой фазы, другое — для возбуждения.
К источнику возбуждения часто относят и устройство для введения анализируемой пробы, вид и конструкция которого зависят от характера, агрегатного состояния и физических свойств пробы. Анализируемые металлические образцы в электрических источниках возбуждения обычно служат электродами разрядного промежутка. Растворы вводят в источник возбуждения с помощью распылителей, порошкообразные пробы – с помощью специальных устройств или при использовании угольных электродов, в которых высверливается канал для набивки порошкообразной пробы. Применяют также брикетирование анализируемого порошка с добавкой металлов, их оксидов или графита. Изготовленный брикет затем становится электродом.
Пламя дает достаточно яркий и стабильный спектр. Возбуждение спектров в пламени имеет в основном термический характер. Температура пламени зависит от состава горючей смеси. Пламя обычной газовой горелки имеет температуру примерно 900°С. Смесь водорода с воздухом дает 2100°С, водорода с кислородом 2800°С, ацетилена с кислородом – около 3000°С.
С помощью пламенных источников определяют свыше 40 элементов (Mg, Сu, Mn, Tl, щелочные элементы, щелочно-земельные и т.д.). В пламени не возбуждаются так называемые трудновозбудимые элементы и общая картина спектра является более простой, чем дугового или искрового. Анализируемое вещество вводится в пламя в виде раствора с помощью специального распылителя, обеспечивающего равномерное поступление вещества.
Электрическая дуга — это электрический разряд при сравнительно большой силе тока (5...7 А) и небольшом напряжении (50...80 В). Разряд поддерживается за счет термоэлектронной эмиссии с раскаленной поверхности катода. Разряд пропускают между электродами из анализируемого образца или между образцом и электродом, не содержащим определяемых элементов. Температура дуги достигает 5000...6000 °С. Введение в электроды примесей, обладающих более низким, чем основной элемент пробы, потенциалом возбуждения понижает температуру дуги. Так, в присутствии солей калия температура дуги между угольными электродами падает с 7000 до 4000 °С. Это открывает возможность регулировать температуру дуги и поддерживать ее постоянной путем введения в зону разряда элемента с низким потенциалом возбуждения – так называемого спектроскопического буфера. Обычно это соли натрия или калия в достаточном количестве. В присутствии спектроскопического буфера устанавливается определенная температура плазмы, практически не зависящая от состава анализируемой пробы.
При анализе тугоплавких металлов и сплавов электроды дуги делают из анализируемого образца. Для анализа легкоплавких металлов и сплавов, а также руд, минералов, стекол, шлаков и других непроводящих материалов электродами служат обычно графитовые или угольные стержни – так называемые спектральные угли. Анализируемая проба помещается в канал одного из электродов и испаряется в плазму при работе дуги.
В дуге удается получить спектр почти всех элементов. Используется дуга постоянного и переменного тока.
Недостатки дуги:
1.
Значительное
разрушение анализируемого образца.
2.
Не всегда
достаточная воспроизводимость условий возбуждения в дуге ограничивает применение
дуговых спектров в основном качественным и полуколичественным анализом. Повышение
напряжения обычно улучшает стабильность дуги, что приводит к повышению точности
анализа. Высоковольтная дуга питается напряжением в несколько тысяч вольт.
Применяют также плазменную горелку или плазмотрон (рис. 3). Плазмотрон представляет собой камеру с двумя графитовыми электродами. В камере между анодом 1 и катодом 3 зажигается дуга при силе тока 20...30 А и по трубке, расположенной по касательной к стенке, подается инертный газ 2 при 150...200 кПа. В аноде имеется отверстие, через которое инертный газ выходит. Вихревые потоки газа в камере охлаждают плазму снаружи, что приводит к сжатию разрядного шнура и увеличению в нем плотности тока. Сжатая плазма вместе с газом выбрасывается через отверстие анода в виде струи длиной 10...15 мм, которая светится над поверхностью анода. Температура в плазме достигает 5000...10 000 °С и выше. Анализируемый раствор 4 подается в плазму специальным распылителем. При анализе твердых образцов пробы могут помещаться в катод или также вводиться в плазму распылителем. Высокая температура и интенсивность свечения делают плазмотрон весьма перспективным источником возбуждения, особенно для анализа трудноиспаряющихся и трудновозбудимых веществ. Большое аналитическое применение находит также высокочастотный плазмотрон с индукционной катушкой, питаемый ВЧ-генератором,
Искра. Для получения искры используют специальные искровые генераторы. Принципиальная схема генератора (рис.4) включает вторичную обмотку повышающего трансформатора 1, которая присоединяется параллельно к емкости 2 и последовательно к катушке самоиндукции 3 и искровому промежутку 4. При горении искры развивается температура 7000...10 000°С и происходит возбуждение всех элементов. При необходимости температура искры может быть повышена до 12000°С и выше. Для проведения локального микроспектрального анализа применяют микроискровой метод, в котором используют игольчатые электроды (например, медные) и устанавливаютмалоемежэлектродное расстояние.
Яркость искрового спектра недостаточна для визуального анализа. Основное достоинство
искры составляет большая стабильность условий разряда и, следовательно,
необходимая в количественном анализе стабильность условий возбуждения. Работа с
искрой практически не вызывает разрушения образца.
Перспективным высокочувствительным источником света является также полый катод, в котором могут возбуждаться элементы с высоким потенциалом возбуждения.
Диспергирующий элемент
Диспергирующий элемент разлагает излучение в спектр. Это наиболее важная часть спектрального прибора, в значительной степени определяющая его аналитические возможности и основные характеристики: линейную дисперсию и разрешающую способность.
Разрешающей способностью спектрального прибора называют его способность давать раздельное изображение двух спектральных линий с близкими длинами волн.
Количественной характеристикой разрешающей способности прибора является
отношение R=l /![]() l , где
l , где ![]() l =l 1-l 2 — интервал, в котором линии l 1 и l 2 наблюдаются раздельно, а l =
l =l 1-l 2 — интервал, в котором линии l 1 и l 2 наблюдаются раздельно, а l =![]() — средняя длина
волны. У обычных спектральных приборов разрешающая способность составляет величину
от 5000 до 50 000.
— средняя длина
волны. У обычных спектральных приборов разрешающая способность составляет величину
от 5000 до 50 000.
В качестве диспергирующего элемента используют призмы, дифракционные решетки и интерференционные устройства. Призмы для спектральных аппаратов изготовляют из стекла или кварца, так как эти материалы достаточно прозрачны в широкой области длин волн. Стеклянные призмы имеют более высокую угловую дисперсию и более доступны по сравнению с кварцевыми, поэтому для работы в видимом и ближнем инфракрасном участках спектра обычно используют стеклянные призмы. Для исследования ультрафиолетовой области спектра применяют призмы из кварца.
Дифракционные решетки в качестве диспергирующего элемента имеют существенные достоинства. Дисперсия света в дифракционной решетке не зависит от длины волны и разрешающая способность решетки значительно выше, чем призмы. Спектральный интервал, доступный для исследования, достаточно широк (от 200 до 1000 нм).
Приемники света
Приемники света характеризуются спектральной чувствительностью: способностью воспринимать излучение различной длины волны и интегральной чувствительностью, которая измеряется действием неразложенного в спектр излучения.
Глаз человека чувствителен к свету в области спектра примерно от 400 до 760 нм. Чувствительность глаза максимальна к желто-зеленому свету (550 нм) и убывает от него в обе стороны — и к красной и к фиолетовой. Возможности глаза как измерительного прибора ограничены также и тем, что он очень приближенно оценивает разность или отношение интенсивностей световых потоков. С достаточной точностью он устанавливает лишь равенство или неравенство интенсивностей световых потоков одного цвета. На этом свойстве основаны все приемы визуальных методов.
Фотопластинка. Светочувствительный слой фотопластинки — это мелкие кристаллы галогенидов серебра, равномерно распределенные в тонком желатиновом слое. При освещении фотопластинки в светочувствительном слое образуется скрытое изображение. Путем обработки фотопластинки проявителем и закрепителем получают изображение спектра в виде спектральных линий.
Другим важным свойством фотопластинки является ее чувствительность. По ГОСТу ее определяют как величину, обратную количеству освещения (экспозиции), необходимого для получения почернения, на 0,2 превышающего почернение вуали при освещении белым светом. Для спектрального анализа более интересной характеристикой является спектральная чувствительность, которую обычно представляют графически как S=f(l ) , где l —длина волны падающего света.
Обычные фотопластинки имеют чувствительность в спектральном диапазоне от 230 до 500 нм. Эти пределы чувствительности могут быть значительно расширены сенсибилизацией пластинок. В настоящее время фотопластинки успешно применяют в широкой спектральной области от короткого ультрафиолета до 1000 нм.
Достоинства фотопластинок:
1.Способность интегрировать интенсивность света.
2.Высокая чувствительность.
3.Достаточно широкий спектральный интервал.
4.Возможность длительное время сохранять информацию, заложенную в спектре.
5.Высокая точность
Недостатки:
1.Неравномерность их эмульсии, представляющая дополнительный источник погрешности анализа.
2.Длительность и трудоемкость операций по химической обработке фотоматериалов.
Фотоэлементы- устройства, преобразующие световую энергию в электрическую. Действие фотоэлементов основано на использовании фотоэффекта. Различают внешний и внутренний фотоэффекты. При внешнем фотоэффекте поглощение света приводит к отрыву электрона с облучаемой поверхности. Внутренний фотоэффект характеризуется увеличением электрической проводимости вещества под действием света. Фотоэлемент с внешним фотоэффектом состоит из фотокатода 1 и анода 2, помещенных в стеклянную колбу 3. Если колба эвакуирована, фотоэлемент называют вакуумным. При действии света на катод (обычно кислородно-цезиевый или сурьмяно-цезиевый) из него вырываются электроны, которые, попадая на анод, замыкают цепь: гальванометр показывает наличие тока.
Достоинства фотоэлементов с внешним фотоэффектом:
1.Чувствительны в широкой области спектра.
2.Имеют линейную световую характеристику.
3.Практически безынерционны.
Недостатки:
1. Невысокая чувствительность.
2.Наличие темнового тока.
3.Хрупкость конструкции.
Значительно более чувствительными приемниками света являются фотоумножители действие которых основано на внешнем фотоэффекте и вторичной электронной эмиссии. Расположение электродов и фокусирующее поле выбирают так, чтобы первичный электронный поток, попадая на первый эмиттер, вызывал вторичную электронную эмиссию, электроны вторичной эмиссии направлялись на следующий эмиттер и т.д. Усиление подчиняется закону геометрической прогрессии:
I=I0 s m
где I — сила тока на выходе прибора; Iо — начальная сила тока;
s — коэффициент вторичной электронной эмиссии; т — число каскадов усиления.
Фотоумножители дают усиление в 105...106 раз.
В фотоэлементах с запирающим слоем используют внутренний фотоэффект полупроводника и вентильный эффект запирающего слоя, который образуется на границе между полупроводником и металлом или двумя полупроводниками. Запирающий слой пропускает электроны практически лишь в одном направлении и не пропускает в другом. Таким образом, возбужденные электроны могут проходить через запирающий слой, создавая разность потенциалов. При замыкании такой системы во внешней цепи появляется ток.
Достоинства фотоэлементов с запирающим слоем:
1.
Высокая
чувствительность.
2.
Широкий
спектральный интервал.
3.
Простота
конструкции.
Недостатки:
1.
Нелинейность
световой характеристики.
2.
Инерционность.
3.
Заметная
температурная зависимость фототока.
КАЧЕСТВЕННЫЙ СПЕКТРАЛЬНЫЙ АНАЛИЗ.
Основой качественного спектрального анализа является свойство каждого
химического элемента излучать характерный линейчатый спектр. Задача качественного
спектрального анализа сводится к отысканию линий определяемого элемента в
спектре пробы. Принадлежность линии данному элементу устанавливается по
длине волны и интенсивности линии. Общее число линий в спектре многих элементов
очень велико. Нет необходимости определять длины волн всех спектральных линий в
спектре пробы. Для целей качественного анализа необходимо установить наличие
или отсутствие в спектре так называемых аналитических или последних линий.
При уменьшении содержания элемента в пробе интенсивность линий этого элемента в спектре будет уменьшаться, некоторые линии исчезнут и число линий уменьшится. При какой-то очень малой концентрации останется всего несколько линий. Это и есть последние линии, по которым обычно проводится качественный анализ. Последние линии хорошо изучены, их длины волн и характеристику интенсивности можно найти в специальных таблицах и атласах спектральных линий. Это обычно, но не всегда резонансные линии. В таблицах их часто отмечают индексами U1 , U2 и т. д. или V1 , V2 и т. д. Индекс U1 показывает, что при возбуждении спектра в дуге эта линия исчезает последней, линия с индексом U2 исчезает предпоследней и т. д. Индексы V1 , Vг и т.д. относятся к этой же последовательности исчезновения линий в искровом спектре. Однако эта последовательность не абсолютна.
В зависимости от условий возбуждения и состава пробы она может несколько изменяться.
Для расшифровки спектра и определения длины волны анализируемой линии пользуются спектрами сравнения, в которых длины волн отдельных линий хорошо известны. Чаще всего для этой цели используют спектр железа, имеющий характерные группы линий в разных областях длин волн.
Спектр анализируемого вещества обычно фотографируют над спектром железа.
Отсутствие последней линии определяемого элемента в спектре гарантирует отсутствие других линий этого элемента. Однако наличие линии с длиной волны, характерной для последней линии какого-либо элемента, еще не означает, что линия действительно принадлежит именно этому элементу. Окончательную идентификацию проводят, проверяя последние линии всех “подозреваемых” элементов.
Спектральным анализом качественно можно определить более 80 элементов. Предел обнаружения методами качественного спектрального анализа колеблется для разных элементов в очень широких пределах: от l0-2 (Hg, Os, U и др.) до 10-5 % (Na, В, Bi и др.). Следует отметить, что отсутствие линии какого-либо элемента в спектре означает лишь, что его концентрация в пробе меньше предела обнаружения. В связи с низким пределом обнаружения методами спектрального анализа нередко “переоткрывают” те или иные элементы, попавшие в пробу в результате случайных загрязнений.
КОЛИЧЕСТВЕННЫЙ СПЕКТРАЛЬНЫЙ АНАЛИЗ.
Перевод компонента твердой пробы в плазму связан с протеканием процессов плавления, испарения и возгонки. На состав плазмы, таким образом, оказывают влияние температура и теплота плавления компонентов пробы, их коэффициенты диффузии, давление пара, температура источника возбуждения и многие другие факторы, поэтому состав вещества в плазме источника возбуждения существенно отличается от состава исходной конденсированной пробы. Недостаточная стабильность условий возбуждения вызывает изменения в составе и температуре плазмы, что приводит к изменению интенсивности спектральных линий и, как следствие, к колебаниям в результатах анализа.
Связь между интенсивностью спектральной линии и концентрацией элемента в пробе при стабильной работе источника возбуждения приближенно устанавливается уравнением (14). Зависимости, наблюдаемые на опыте, хорошо описываются уравнением Ломакина (15). Коэффициент самопоглощения b в этом уравнении зависит от концентрации, однако в некотором, иногда довольно широком интервале концентраций он остается постоянным.
В практике количественного спектрального анализа обычно используют интенсивность не отдельной линии, а отношение интенсивностей двух спектральных линий, принадлежащих разным элементам. Таким образом, в качестве свойства, связанного с концентрацией элемента, используется отношение интенсивности линии определяемого элемента к интенсивности линии другого элемента в этом же спектре. Такая методика позволяет снизить требования к постоянству условий возбуждения и регистрации спектров.
Линию определяемого элемента обычно называют аналитической линией и ее интенсивность обозначают Ia или называют линией примеси и обозначают интенсивность Iпр Вторую линию, обычно называемую линией сравнения, выбирают так, чтобы отношение интенсивностей зависело только от концентрации определяемого элемента, но не от условий возбуждения и регистрации спектра. Иногда в анализируемую пробу специально вводят так называемый внутренний стандарт, т.е. элемент, линию которого используют в качестве линии сравнения.
Уравнение Ломакина (15) для аналитической линии и линии основы имеет вид
Iпр=a’ cbпр (15)
а отношение
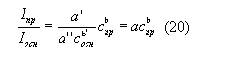
Уравнение (20) показывает, что отношение интенсивностей также пропорционально концентрации элемента в пробе. Это основное уравнение методов количественного спектрального анализа. Методы различаются лишь способом оценки относительной интенсивности. При выборе пары линий для количественного анализа руководствуются рядом требований к энергиям возбуждения спектральных линий, их длинам волн и интенсивностям. Выполнение этих требований существенно уменьшает зависимость относительной интенсивности от условий возбуждения.
В зависимости от способа оценки интенсивностей различают следующие методы
количественного спектрального анализа:
1)визуальные; 2)фотографические; 3)фотоэлектрические.
При классификации методов спектрального анализа в отдельную группу выделяют так называемый полуколичественный спектральный анализ.
Полуколичественный спектральный анализ
Обычная погрешность полуколичественных спектральных методов составляет 10% или более. Однако когда простота и экспрессность важнее точности, эти методы применяют очень широко. Оценку интенсивности спектральных линий в полуколичественном анализе производят визуально, наблюдая спектр или непосредственно в окуляре спектрального прибора, или на фотопластинке.
Наиболее распространенным методом полуколичественного анализа является метод гомологических пар, или, как его иногда называют, метод однородных дублетов. Для проведения анализа этим методом предварительно подбирают пару линий (голомогическую пару или однородный дублет) и устанавливают, при какой концентрации определяемого элемента их интенсивности одинаковы.
Предел обнаружения составляет обычно 0,01... ...0,10%, погрешность около ±20% (относительных). Успешно применяется стилоскоп, более высокая точность результатов достигается с помощью стилометра.
Из фотографических методов полуколичественного анализа применяют метод спектров сравнения и метод появления или исчезновения чувствительных линий. В методе спектров сравнения на одной пластинке фотографируют спектры нескольких эталонов и спектр пробы, а затем сравнивают на глаз почернение линий определяемого элемента в полученных спектрах. Такое сравнение позволяет установить пределы концентраций анализируемого элемента. В методе появления или исчезновения линий сначала с помощью эталонов устанавливают, при каких концентрациях появляются или исчезают те или иные чувствительные линии элементов, а затем, используя полученные данные, находят ориентировочное содержание элемента в пробе.
Фотографические
методы количественного анализа.
При рассмотрении свойств фотопластинки было установлено, что почернение S
связано с освещенностью Е уравнением (19). В условиях спектрального
анализа Е =I : S=g
lgI+g lgt - i
При постоянной выдержке последние члены правой части этого уравнения постоянны, поэтому
S=g lgI+const (25)
![]()
Запишем уравнение для почернения линии примеси и линии основы и вычтем одно из другого:
При логарифмировании уравнения (20) имеем
![]()
Объединяя уравнения (26) и (27), получаем
![]() S = g lg a + g b lg cпр
(28)
S = g lg a + g b lg cпр
(28)
Это основное уравнение фотографических методов количественного спектрального анализа.
Относительная ошибка в концентрации не зависит от абсолютного значения ![]() и уменьшается при
увеличении g и b. Для ориентировочных
подсчетов в области оптимальных почернении примем b = 0,7, d(
и уменьшается при
увеличении g и b. Для ориентировочных
подсчетов в области оптимальных почернении примем b = 0,7, d(![]() S) = 0,02,
g = 1,3. Относительная погрешность при
этих условиях составляет ~5%.
S) = 0,02,
g = 1,3. Относительная погрешность при
этих условиях составляет ~5%.
Наиболее распространенным из фотографических методов количественного
спектрального анализа является метод трех эталонов. Сущность его
заключается в следующем. На одной пластинке фотографируются спектры
анализируемого образца и трех эталонов. Для анализа массовых проб (стали,
сплавы и т. д.) применяют специальные наборы эталонов, которые выпускает
лаборатория стандартных образцов. По спектрам эталонов строят градуировочный
график. Для повышения точности спектры эталонов и образца фотографируют 2...3
раза и берут средние значения ![]() S.
S.
В методе постоянного графика удается согласовать измерения, сделанные на различных пластинках, и построить постоянный график
Опыт показал, что неконтролируемые изменения условий возбуждения вызывают сдвиг градуировочного графика. Так как сдвинутый график, как правило, оказывается параллельным первоначальному, то для учета сдвига одновременно со спектром образца фотографируют спектр контрольного эталона. Через точку, соответствующую этому эталону, проводят прямую, параллельную первоначальному графику, которая и будет истинным градуировочным графиком для образцов на данной пластинке. Это твердый график и метод называют методом твердого графика или контрольного эталона.
Рис 9. Градуировочный график в методе добавок
В практике спектрального анализа применяют также метод добавок, особенно при анализе немассовых проб сложного состава и исследованных чистых и сверхчистых веществ. При анализе по этому методу пробу обычно переводят в раствор и делят его на несколько частей. Затем в каждую часть добавляют разное, но точно известное количество определяемого элемента, снимают спектр и определяют интенсивность спектральных линий. Для расчета строят график, основываясь на том, что в области малых концентраций достаточно хорошо выполняется линейная зависимость Iпр/Iосн= ас, так как с уменьшением концентрации самопоглощение существенно падает. При этом, если с—неизвестная концентрация, а cст—концентрация введенного стандарта, то
Iпр/Iст=а(сx+Сст). (30)
Откладывая на графике Iпр/Iст как функцию cст,
получают прямую, пересекающую ось ординат при cст = 0 (рис. 9).
Экстраполяция этой прямой до пересечения с осью абсцисс дает отрезок на оси,
равный —cх. Действительно, при Iпр/Iосн
=0 из уравнения (30) следует, что — cст=cх.
ФОТОМЕТРИЯ ПЛАМЕНИ (ПЛАМЕННАЯ ЭМИССИОННАЯ СПЕКТРОСКОПИЯ).
Фотометр для фотометрии пламени имеет источник возбуждения (пламенная горелка), диспергирующий элемент (обычно светофильтр) и приемник света—рецептор (обычно фотоэлемент). В спектрофотометрах для пламени вместо светофильтров применяют призмы и дифракционные решетки. Анализируемый раствор в пламя горелки вводится в виде аэрозоля. При этом растворитель испаряется, а соли металлов диссоциируют на атомы, которые при определенной температуре возбуждаются. Возбужденные атомы, переходя в нормальное состояние, излучают свет характерной частоты, который выделяется с помощью светофильтров, и его интенсивность измеряется фотоэлементом.
Количественные определения проводят методом градуировочного графика или методом добавок. Методы фотометрии пламени характеризуются низким пределом обнаружения (до 0.001 мкг/мл для щелочных металлов и 0,1 мкг/мл для других) при погрешности 1...3%. Этим методом могут быть определены Li, Na, К, Rb, Cs, Sr, Ba, Ca, In, Ag и другие элементы.
Достоинств метода фотометрии пламени:
1.Высокая производительность.
2.Спектры, получаемые в пламени, более просты, чем дуговые или искровые, так как температура пламени ниже, чем в электрических источниках возбуждения.
Недостатки:
1.Небольшое число определяемых элементов.
ПРАКТИЧЕСКОЕ ПРИМЕНЕНИЕ.
Области применения:
1. В металлургической промышленности (исходное сырье, готовая продукция, спектрально-аналитический контроль за ходом плавки).
2.При анализе геологических проб при поиске полезных ископаемых.
3.Для контроля технологического процесса на горно-обогатительных и гидрометаллургических предприятиях
4.Анализ природных и сточных вод, почвы, атмосферы и других объектов окружающей среды, а также в медицине и биологии.
5.Анализ чистых материалов в электронной технике и других областях, анализ реактивов и т. д.
6.В космических исследованиях
ОБЩАЯ ХАРАКТЕРИСТИКА МЕТОДА
Достоинства:
1. Низкий предел обнаружения. Средний предел обнаружения методами эмиссионной
спектроскопии составляет 10-3...10-4% (до 10-5),
а при использовании приемов обогащения он снижается до 10-5…10-7%
.
2. Точность. Погрешность определения характеризуется в среднем величиной 1...2%.
3. Экспрессность.
4. Универсальность.