Отличительные
особенности аналитического контроля микрокомпонентов в объекте ОС от контроля
компонентов матрицы.
Концентрирование в аналитической химии,
частный случай разделения компонентов исследуемой смеси, в результате к-рого
повышается отношение концентрации (кол-ва) микрокомпонентов к концентрации
(кол-ву) макрокомпонента. При этом можно или удалять матрицу, или выделять микрокомпонент.
Главное достоинство концентрирования - снижение относительных, а иногда и абс.
пределов обнаружения микрокомпонентов благодаря устранению или резкому
уменьшению влияния матрицы на результаты определения. В ряде случаев удается
повысить точность анализа, упростить градуировку концентрирования полезно при
анализе токсичных, радиоактивных и дорогостоящих в-в и материалов. Однако оно усложняет
и удлиняет анализ, иногда ухудшает метрологич. параметры методик. Различают
абсолютное и относительное концентрирование. В первом случае микрокомпоненты
переводят из большого объема в малый и их концентрация повышается, как, напр.,
при отгонке Н2О в ходе анализа прир. вод. Во втором случае
увеличивается лишь соотношение между концентрациями микрокомпонентов и мешающих
макрокомпонентов (к к-рым не относят р-ритель). При индивидуальном
концентрировании из образца выделяется один или последовательно неск.
микрокомпонентов, а при групповом - неск. микрокомпонентов одновременно.
Количественно концентрирование характеризуют степенью извлечения R, коэф.
концентрирования К и коэф. разделения S=1/К. Степень извлечения показывает,
какая доля от абс. кол-ва микрокомпонента выделена в концентрат:
R= qкqпр или
R(в%)=qк.100/qпр,
где qк и qпр -
абс. кол-ва определяемого микрокомпонента соотв. в концентрате и пробе. Коэф.
концентрирования показывает, во сколько раз изменилось отношение абс. кол-в
микрокомпонента и матрицы при концентрировании:
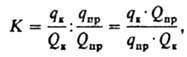
где Qк и Qпр -
абс. кол-ва матрицы соотв. в концентрате и пробе. Для концентрирования
применяют разл. методы: экстракцию, жидкостную и газовую хроматографию; сорбцию
(адсорбцию, абсорбцию, хемосорбцию); избират. растворение, осаждение и
соосаждение; методы, основанные на разл. электрохим. поведении макро- и
микрокомпонентов (гл. обр. электровыделение, электродиализ, электрофорез,
электроосмос); отгонку, ректификацию и мол. дистилляцию, сублимацию,
кристаллизацию (направленную кристаллизацию и зонную плавку); пробирную плавку;
флотацию; фильтрование, диализ и др. Часто различают комбинированные и
гибридные методы. В комбинир. методах концентрирование и определение -
последоват. стадии анализа, и концентрат (или продукт разделения) необходимо
переводить в форму, пригодную для определения. В гибридных методах
концентрирование (и разделение) и определение тесно и гармонично связаны, как,
напр., в газовой хроматографии, а концентрат (продукт разделения) анализируется
без дополнит. обработки. Концентрирование широко применяют при определении
микрокомпонентов в объектах окружающей среды, минер, сырье, металлах и сплавах,
в-вах высокой чистоты. наиб. распространение для анализа концентратов получили
такие методы, как фотометрия, атомно-эмиссионный, атомно-абсорбционный,
рентгенофлуоресцентный и нейтронно-активационный анализ, инверсионная вольтамперометрия.
Орг. микрокомпоненты удобно определять газовой и жидкостной хроматографией,
хромато-масс-спектрометрией. Для концентрирования газообразующих микроэлементов
широко применяют высокотемпературную экстракцию.
Разделение осаждением и соосаждением
В основе всех разделений методом осаждения
лежит различие в растворимости соединений определяемого и мешающего
(нежелательного) элементов. Возможность и условия эффективного разделения
главным образом определяются величинами произведений растворимости ПР.
Для количественного разделения неорганических
веществ (здесь мы рассматриваем в основном эти соединения) используют множество
осадителей. Известно, что растворимость гидроксидов, гидратированных оксидов и кислот
разных элементов заметно различается.
Если учесть к тому же, что рН растворов
можно изменять на 14 и более единиц (т.е. в более, чем 1015 раз) при помощи
различных буферных растворов, то разделения, основанные на регулировании величин
рН, легко осуществимы. Эти методы можно разделить на три основные группы (в
зависимости от рН):
а) разделения в достаточно
концентрированных растворах сильных кислот;
б) разделения в присутствии буферных растворов
в большом контролируемом интервале значений рН;
в) разделения в относительно концентрированных
растворах гидроксидов щелочных металлов (калия, натрия и др.).
Соосаждение
Соосаждение
− это процесс распределения микрокомпонента между раствором (жидкая фаза)
и осадком (твердая фаза) без образования собственной твердой фазы. Различают
несколько видов соосаждения: адсорбцию, окклюзию, образование твердого раствора
(изоморфное соосаждение).
Причиной
адсорбции принято считать нескомпенсированность заряда ионов на поверхности
кристаллов. Это экзотермический процесс, т.е. в данном случае повышение температуры
снижает степень загрязненности осадка.
Окклюзия − основной вид загрязнения
осадков. Вид и количество примесей в осадке зависит от скорости его формирования
и порядка сливания растворов. Например, сульфат бария можно получить, приливая
серную кислоту к раствору соли хлорида бария, и наоборот. В первом случае образующиеся
кристаллы сульфата бария будут адсорбировать в процессе роста ионы бария и в качестве
противоионов Cl−, т.е. осадок будет преимущественно окклюдировать
хлорид бария (возможна небольшая окклюзия и серной кислоты). При осаждении BaSO4
путем добавления к раствору серной кислоты раствора хлорида бария кристаллы
сульфата бария адсорбируют сульфат-ионы и в качестве противоионов − Н3О+,
осадок окклюдирует преимущественно серную кислоту (при этом возможна некоторая
окклюзия хлорида бария).
Экстракция
Экстракция
− это распределение вещества между двумя обычно несмешивающимися фазами
(обычно между водой и каким−нибудь органическим растворителем). Экстракция
( это также метод выделения, разделения и концентрирования веществ.
При экстракции одновременно протекает несколько
процессов:
а) образование экстрагируемых
соединений;
б) распределение экстрагируемых соединений
между водной и органической фазами;
в) реакции в органической фазе
(диссоциация, ассоциация, полимеризация).
Вещество (обычно в органической фазе),
образующее экстрагируемое соединение, называют экстрагентом, а инертные органические
растворители, применяемые для улучшения физических и экстракционных свойств
экстрагента, называют разбавителями (обычно это хлороформ, тетрахлорид
углерода, бензол и др.). Органическая фаза, отделенная от водной фазы, содержащая
экстрагированные соединения, называется экстрактом.
Можно еще добавить, что обратный перевод
вещества из органической фазы в водную называют реэкстракцией. Экстракционные
методы выделения веществ нашли широкое применение при анализе компонентов некоторых
промышленных и природных объектов. Экстракция выполняется достаточно быстро, при
этом достигается высокая эффективность разделения и концентрирования, пожалуй, легко
совместима с разнообразными методами анализа. Многие аналитически важные методы
экстракции стали прообразами важных технологических экстракционных процессов, особенно
в атомной энергетике.
Хроматография
Более широкие возможности открываются
при использовании в хроматографах реакционной газовой хроматографии по причине
того, что многие нелетучие, термонеустойчивые или агрессивные вещества
непосредственно перед введением в хроматографическую колонку могут быть
переведены с помощью химических реакций в другие — более летучие и устойчивые.
Чаще всего химические превращения осуществляют на входе в колонку хроматографа,
реже – в самой колонке или на выходе из нее перед детектором. Более удобно
проводить превращения вне хроматографа. К недостаткам метода реакционной
газовой хроматографии следует отнести возрастание времени анализа и появление
новых источников ошибок.
Метод реакционной хроматографии часто
применяют в хроматографах для определения содержания микроколичеств воды. Вода
реагирует с гидридами металлов, с карбидом кальция или металлическим натрием и
др., продукты реакции (водород, ацетилен) детектируются с высокой
чувствительностью пламенно-ионизационным детектором. К парам воды этот детектор
малочувствителен. Широко применяют химические превращения в анализе термически
неустойчивых биологических смесей