Аренкарбальдегиды получают окислением метиларенов и бензиловых спиртов.
![]()
![]()
Окислители: CrO3 + (CH3CO)2O; CrO2Cl2
При окисление других алкиларенов образуются алкиларилкетоны.
![]()
Окислители: О2 в присутствии катализаторов – солей кобальта и марганца.
Окисление диарилметанов дает диарилкетоны.
![]()
Окислители: KMnO4; CrO3.
2) Гидролиз дигалогеналкиларенов
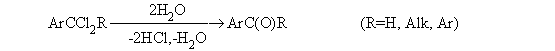
3) Ацилирование аренов
![]()
4) Формилирование аренов
Для формилирования (введения группы СНО) необходим хлорангидрид муравьиной кислоты, который крайне нестабилен и разлагается на СО и НCl, поэтому используют другие формилирующие реагенты
Реакция Гаттермана-Коха. Формилирование по Гаттерману-Коху осуществляется под действием оксида углерода (II) и хлористого водорода в присутствии катализатора Фриделя-Крафтса - хлорида алюминия, промотированного хлоридом меди (I).
![]()
Роль однохлористой меди в этой реакции неясна: возможно она связывает СО в комплекс, что способствует образованию крайне нестабильного хлористого формила HCOCl из CO и HCl. Таким путем удается ввести альдегидную группу в алкилбензолы, арилгалогениды, полициклические углеводороды, причем формильная группа вводится селективно в пара-положение. Реакция не применима для формилирования фенолов, их эфиров и ариламинов.
Реакция Гаттермана. В качестве формилирующего агента используется смесь безводного HCN и газообразного хлористого водорода в присутствии кислоты Льюиса.
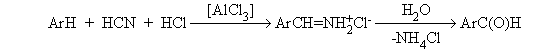
Электрофильным реагентом является, вероятно, комплекс катализатора с формимидхлоридом.
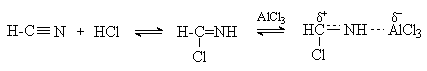
Образующийся в синтезе гидрохлорид альдимина ArCH=NH2+Cl гидролизуют до альдегида.
Для того, чтобы избежать применения ядовитой синильной кислоты, Р.Адамс модифицировал реакцию, заменив синильную кислоту цианидом цинка (реакция Гаттермана-Адамса). Это позволило из цианида цинка и HCl получать непосредственно в реакционной смеси HCN и безводный хлористый цинк, играющий роль слабой кислоты Льюиса. Этот метод дает хорошие результаты при формилировании фенолов и простых эфиров фенолов.
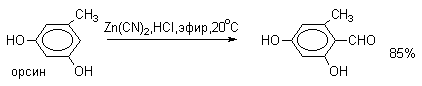
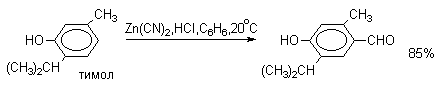
Реакции Гаттермана и Гаттермана-Адамса используют также для формилирования алкилбензолов и конденсированных ароматических углеводородов. Метод не применим для аренов, содержащих дезактивирующие заместители, и ароматических аминов.
Реакция Вильсмейера-Хаака. В качестве формилирующего реагента используют диметилформамид (ДМФА) в присутствии POCl3 как кислоты Льюиса.
![]()
Электрофильным агентом в реакции Вильсмейера-Хаака является иминиевая соль, которая образуется при взаимодействии ДМФА и хлорокиси фосфора (см. лек.29).
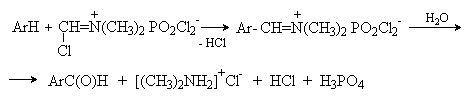
Реакция Вильсмейера-Хаака чрезвычайно проста в экспериментальном отношении и обеспечивает очень высокие выходы ароматических альдегидов, содержащих NR2-,OR- или OH-группы. Она оказывается практически ценной при формилировании конденсированных ароматических углеводородов - антрацена, азулена, пирена и др., а также разнообразных гетероциклических соединений ряда фурана, тиофена, пиррола, индола.
Реакция Реймера-Тимана. Используется для формилирования фенолов.
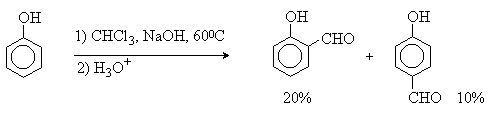
Подробнее см. лек.№29.
5) Восстановление хлорангидридов аренкарбоновых кислот (реакция Розенмунда)
![]()
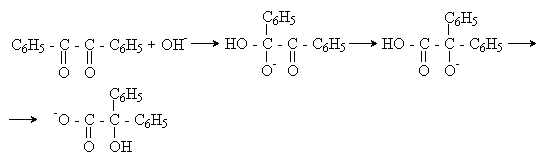
При нагревании в присутствии цианидов аренкарбальдегиды образуют a -гидроксикетоны (бензоины).
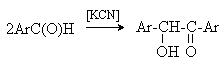
Механизм реакции:
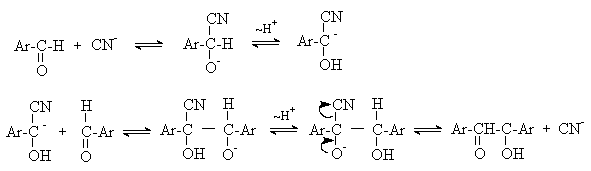
Ключевая стадия процесса – образование карбаниона за счет миграции протона от атома углерода к атому кислорода, которая становится возможной благодаря электроноакцепторному действию цианогруппы.
б) Реакция Канницаро
Аренкарбальдегиды, как альдегиды, не содержащие a -водородных атомов, вступают в реакцию Канницаро.
2ArC(O)H + NaOH ® ARCOONa + ARCH2OH
Подробнее см. лек.№31-33.
в) Реакция Перкина
Аренкарбальдегиды конденсируются с ангидридами карбоновых кислот в присутствии оснований (ацетатов и карбонатов щелочных металлов, пиридина). При этом альдегид выполняет роль карбонильной, а ангидрид – метиленовой компоненты.
![]()
Механизм реакции:
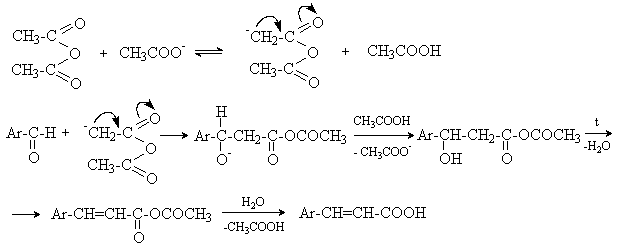
г) Автоокисление
Аренкарбальдегиды очень легко окисляются кислородом воздуха на свету.
ArCHO + 1/2O2 ® ArCOOH
Процесс протекает по свободнорадикальному механизму через промежуточное образование стабильных ароильных радикалов Ar-C. =O.
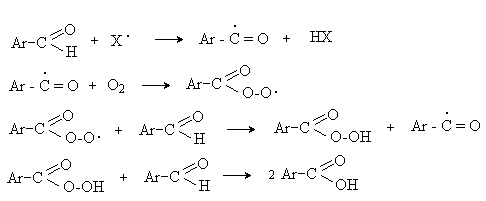
д) Хлорирование
Аренкарбальдегиды легко хлорируются по свободнорадикальному механизму с образованием хлорангидридов.
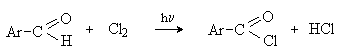
Механизм:
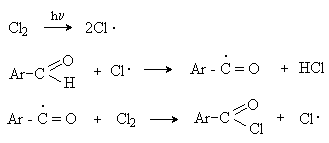
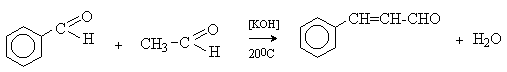
а при конденсации с с ацетофеноном – халкон:
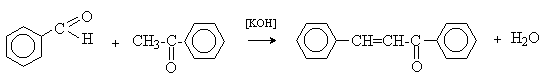
Коричный альдегид обладает свойствами a,b-непредельных карбонильных соединений. Используется в парфюмерии и пищевой промышленности.
Бензофенон – бесцветное кристаллическое вещество. В промышленности его получают окислением дифенилметана. Для бензофенона характерно образование стабильного анион-радикала синего цвета при взаимодействии с металлическим натрием.
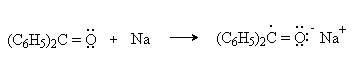
Такие анион-радикальные соли называют металлкетилами. Их относительная устойчивость связана со стабилизирующим влиянием на свободнорадикальный центр двух бензольных ядер и отрицательно заряженного атома кислорода.
Дибензоил – желтое кристаллическое вещество. Образуется при окислении бензоина.
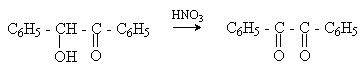
При нагревании со спиртовым раствором щелочи дибензоил претерпевает перегруппировку с образованием бензиловой кислоты (бензиловая перегруппировка).
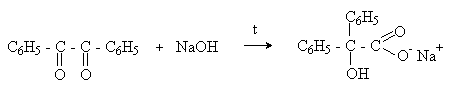
Механизм: