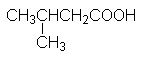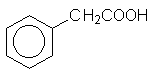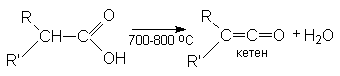Лекция №35
КАРБОНОВЫЕ КИСЛОТЫ
План.
- Классификация,
номенклатура.
- Методы
получения насыщенных карбоновых кислот.
- Строение,
физические и химические
свойства насыщенных монокарбоновых кислот.
Карбоновые
кислоты являются производными углеводородов, в которых один или несколько
атомов водорода замещены на карбоксильную группу.
Карбоновые кислоты можно подразделить на две основные группы:
- Монокарбоновые
кислоты (насыщенные, ненасыщенные, аренкарбоновые кислоты).
- Ди- и
поликарбоновые кислоты (ненасыщенные, насыщенные, арендикарбоновые и
поликарбоновые кислоты).
Монокарбоновые кислоты
Классификация , изомерия и номенклатура
Монокарбоновые
кислоты подразделяют в зависимости от природы углеводородного остатка.
a) Насыщенные монокарбоновые кислоты (производные алканов и циклоалканов):
CnH2n+1COOH , 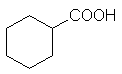
б) Ненасыщенные монокарбоновые кислоты (производные алкинов, алкенов, алкадиенов и других ненасыщенных углеводородов,
CnH2n-1COOH
, CnH2n-3COOH и др.
в) Аренмонокарбоновые кислоты
ArCOOH,
ArCH2COOH, ArCH=CHCOOH
Согласно номенклатуре IUPAC название карбоновых кислот образуют от названия родоначальных углеводородов с тем же числом атомов углерода, включая и атом карбоксильной группы, и окончания “–овая кислота”.
Нумерацию начинают от атома углерода
карбоксильной группы. Многие карбоновые кислоты сохраняют тривиальные названия.
Иногда название карбоновой кислоты образуют от названия углеводорода,
содержащего карбоксильную группу в качестве заместителя. Примеры образования
названий в карбоновых кислот приведены ниже
|
Формула |
Тривиальные названия |
Названия в системе IUPAC |
Названия с окончанием “карбоновая кислота” |
|
HCOOH |
Муравьиная кислота |
Метановая кислота |
|
|
CH3COOH |
Уксусная кислота |
Этановая кислота |
|
|
CH3CH2COOH |
Пропионовая кислота |
Пропановая кислота |
|
|
CH3CH2CH2COOH |
Масляная кислота |
Бутановая кислота |
|
|
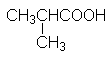
|
Изомасляная кислота |
2-Метил-пропановая кислота |
|
|
CH3CH2CH2CH2COOH |
Валериановая кислота |
Пентановая кислота |
|
|
|
Изовалериановая кислота |
3-метилбу-тановая кислота |
|
|
(CH3)3C-COOH |
Пивалоновая кислота |
2,2-диметил-пропановая кислота |
2-метилпропан-карбоновая-2-кислота |
|
CH3(CH2)4COOH |
Капроновая кислота |
Гексановая кислота |
|
|
CH3(CH2)16COOH |
Стеариновая кислота |
Октадекановая кислота |
|
|
|
|
|
Циклогексанкарбо-новая кислота |
|
CH2=CH-COOH |
Акриловая кислота |
Пропеновая кислота |
Этиленкарбоновая кислота |
|
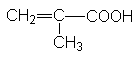
|
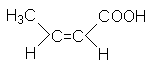
Метакриловая кислота |
2-Метилпропеновая кислота |
Пропенкарбоновая-2 кислота |
|
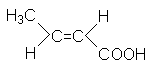
|
Кротоновая кислота |
транс-Бутен-2-овая кислота |
|
|
|
Изокротоновая кислота |
цис-Бутен-2-овая кислота |
|
|
|
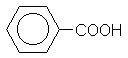
Бензойная кислота |
|
Бензолкарбоновая кислота |
|
|
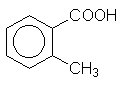
о-Толуиловая кислота |
|
o-Толуолкарбоновaя кислота |
|
|
Фенилуксусная кислота |
Фенилэтановая кислота |
|
|
|
Коричная кислота |
транс-3-фенилпропеновая кислота |
|
Методы получения насыщенных монокарбоновых кислот
1. Окисление первичных спиртов и альдегидов.
В промышленном масштабе окисление ведут кислородом воздуха при катализе солями марганца или кобальта
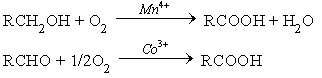
В лаборатории окисление осуществляют неорганическими окислителями: KMnO4 в кислой или нейтральной среде, K2Cr2O7 в кислой среде.
2. Окисление неразветвленных алкенов
![]()
Окислителями являются K2Cr2O7 в кислой среде или KMnO4 в кислой среде.
3. Окисление алкинов.
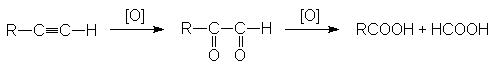
В качестве окислителей используют те же реагенты, что и при окислении алкинов.
4.Окисление алканов (промышленный метод)
RCH2CH2R' + 5/2O2 ® RCOOH + R'COOH + H2O
Окисление осуществляют при катализе реакции солями кобальта или марганца.
5. Гидролитические методы.
а) Кислотный гидролиз нитрилов
RCº N + 2H2O + HX ® RCOOH + NH4X
б) Основной гидролиз нитрилов
RCº N + H2O + NaOH ® RCOONa + NH3
в) Кислотный гидролиз амидов кислот
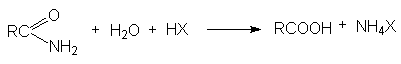
г) Основной гидролиз амидов кислот
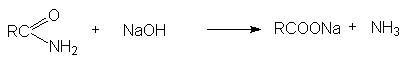
д) Кислотный гидролиз сложных эфиров
![]()
е) Основной гидролиз сложных эфиров
RCOOR' + NaOH ® RCOONa + R'OH
ж) Гидролиз ангидридов карбоновых кислот
(RCO)2O + H2O ® 2RCOOH
з) Гидролиз галогенангидридов карбоновых кислот
RCOHal + H2O ® RCOOH + HHal
и) Гидролиз соединений, содержащих трихлорметильную группу
RCCl3 + 2H2O ® RCOOH + 3HCl
Гидролиз осуществляет либо основанием, либо водой при катализе апротонными кислотами, например, FeCl3.
6. Металлоорганический синтез.
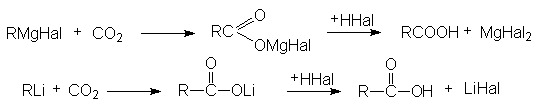
7. Реакции карбонилирования
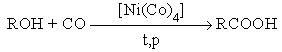
8. Гидрокарбоксилироание галогеналканов и алкенов.
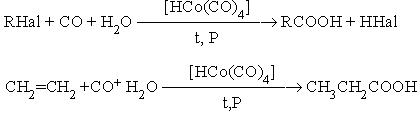
9. Синтез Арндта-Эйстерта
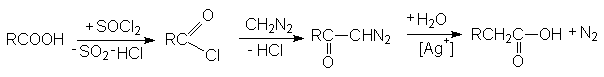
диазокетон
Эта реакция представляет собой удобный способ
превращения карбоновой кислоты RCOOH в ее ближайший гомолог RCH2COOH.
Технически важную муравьиную и уксусную кислоты получают следующими способами.
Муравьиная кислота и ее эфиры:
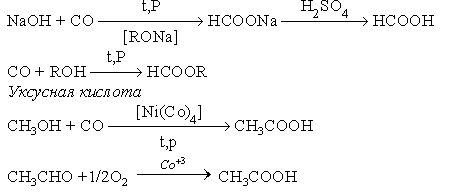
Физические свойства и строение
монокарбоновых кислот
Насыщенные монокарбоновые кислоты представляют собой бесцветные жидкие или кристаллические вещества с острым своеобразным запахом, высшие карбоновые кислоты (С15 – С18) имеют слабый запах стеарина. Они имеют весьма высокие температуры кипения, что свидетельствует о значительной межмолекулярной ассоциации следствие образования межмолекулярных водородных связей, причем образуются как циклические димеры, так и линейные олигомеры.
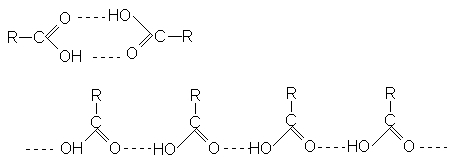
Электронографическое изучение карбоновых кислот показало, что в их молекуле имеются карбонильная и гидроксильная группа, при этом связь С = О длиннее, чем в кетонах, а связь С – О короче, чем в спиртах. Это свидетельствует о сопряжении неподеленной пары кислорода гидроксильной группы и орбиталей карбонильной группы
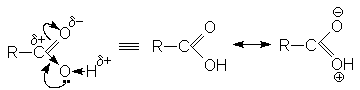
Проявляя +М – эффект, атом кислорода гидроксильной группы увеличивает полярность связей ОН, но в то же время в некоторой степени уменьшает положительный заряд на углеродном атоме по сравнению альдегидами и кетонами. Одновременно действует электроноакцепторный индуктивный эффект (-I) кислородных атомов.
Таким образом в карбоксильной группе имеется сильно поляризованный положительно атом водорода гидроксильной группы и углеродный атом которые являются нуклеофильными центрами. В то же время кислородный атом имеет нуклеофильный характер.
Химические свойства карбоновых кислот
Большинство реакций карбоновых кислот может быть отнесено к одному из четырех основных типов:
1.Реакции, сопровождающиеся разрывом
О-Н-связей, например, кислотная диссоциация.
2.Реакции по карбонильному углероду, которые имеют нуклеофильный характер.
3.Реакции расщепления
4.Реакции по a -углеродному атому алкильной группы.
Кислотность карбоновых кислот
По сравнению со спиртами карбоновые кислоты обладают более высокой кислотностью. При этом в растворе реализуется равновесие.
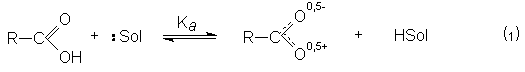
Способность к отдаче к протонам обусловлена двумя факторами: поляризацией связей О-Н в исходном состоянии и стабилизацией карбоксилат-аниона из-за деколализации отрицательного заряда в нем посредством резонанса.
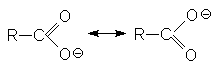
Кислотность карбоновых кислот характеризуется константой кислотности Ка или показателем рКа. Их значения обычно составляет приблизительно 10-5, что свидетельствует о слабости этих кислот. Присутствие в структуре радикала электроноакцепторных заместителей будет стабилизировать карбоксилат анион, что приведет к увеличению кислотности соответствующей ему кислоты. Например: рКа монохлоруксусной кислоты составляет 2,9 а уксусной – 4,8. По мере удаления электроноакцепторного заместителя от карбоксильной группы кислотность снижается, что связано с быстрым затуханием индуктивного эфекта: так рКа b -хлорпропионовой кислоты составляет ~4,0. Наоборот, увеличение разветвления алкильного радикала приводит к снижению кислотности, так как при этом возрастает индуктивный эффект алкильной группы. На основе этих данных можно представить следующие ряды кислотности карбоновых кислот.
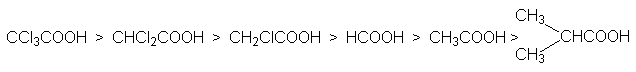
![]()
Кислотность карбоновых кислот проявляется в их взаимодействии с активными металлами и основаниями.
2RCOOH +
2Na ® 2RCOONa + H2
RCOOH +
NaOH ® RCOONa + H2O
2RCOOH +
Na2CO3 ® 2RCOONa + H2O + CO2
Основность карбоновых кислот
В кислой среде (pH<3) диссоциация карбоновых кислот практически не происходит, так как равновесие (1) существенно смещено в левую сторону из-за избытка ионов HSolÅ . В то же время в кислой среде осуществляется протонирование карбоновых кислот по основному карбонильному кислороду.
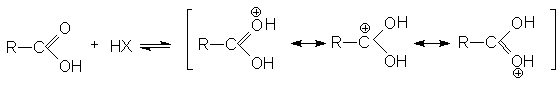
В протонированной форме оба кислородных атомов становятся одинаковыми:
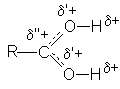
Несмотря на малую концентрацию протонированной формы присутствие небольших количеств сильных кислот исключительным образом влияет на реакционную способность карбоновых кислот: повышение положительного заряда на карбонильном углероде делает его восприимчивым к атаке нуклеофильными реагентами и открывает возможность для протекания многих реакций нуклеофильного замещения карбоновых кислот.
Реакции нуклеофильного замещения
1.Реакции этерификации
![]()
В
механизме этой реакции ключевую роль играет протонирование карбоновой кислоты
кислотой-катализатором.
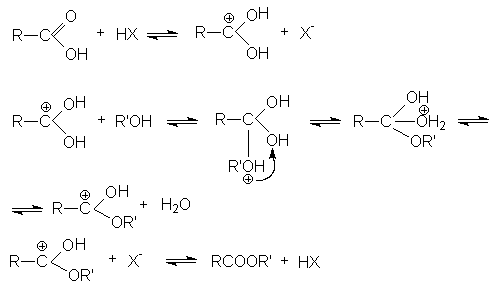
Реакция этерификации может осуществляться некаталитически, однако для этого требуется жесткие условия процесса.
2. Реакции с N-нуклеофилами
(аммиаком, аминами, гидразином и др.).
N-нуклеофилы
при взаимодействии с карбоновыми кислотами как правило образуют аммониевые соли
(карбоксилаты) и только при повышенных температурах происходит присоединение
N-нуклеофила к карбонильному углероду.
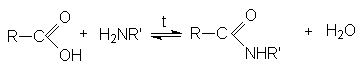
Механизм реакции согласуется с общепринятыми представлениями о механизме нуклеофильного присоединения азотистых оснований по карбонильной группе:
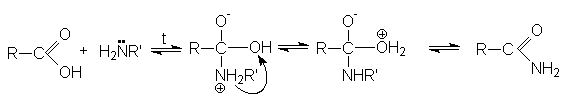
3. Взаимодействие с галогенангидридами хлорорганических кислот (PCl3, PCl5, PBr3, SOCl2 ).
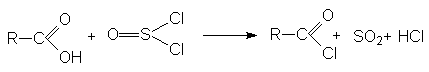
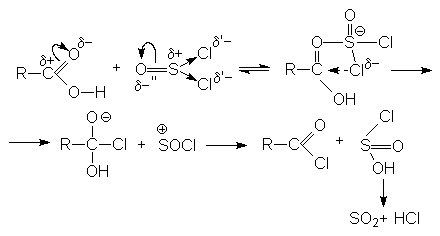
Механизм реакции связан с концертной атакой электрофильного и нуклеофильного центров карбоновой кислоты молекулой галогенангидрида:
Реакции расщепления
1. Синтез Кольбе (см. подробно
методы получения алканов).
![]()
2. Пиролиз карбоновых кислот.
3. Реакция Хунсдиккера.
RCOOAg + Br2 ® RBr + CO2 + AgBr
В
качестве объекта декарбоксилирования выступают серебряные или ртутные соли
карбоновых кислот, а реагентами являются бром или йод.
Предполагают, что промежуточным продуктом этой реакции является гипогалогенит, который распадается на радикалы:
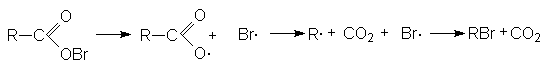
Эту реакцию можно осуществлять без выделения чистых солей ртути или серебра
2RCOOH +
HgO + 2Br2 ® 2RBr + HgBr2
+ H2O + 2CO2
4. Пиролитическая кетонизация солей
карбоновых кислот
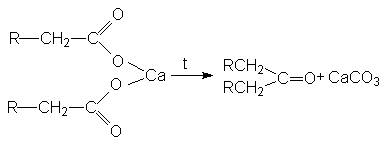
Галогенирование по Гелю-Форгальду-Зелинскому
Эта реакция является примером взаимодействия по a -углеродному атому по отношению к карбоксильной группе. Реакция бромирования протекает энергично и с хорошим выходом в присутствии небольших количеств фосфора.
![]()
Функция фосфора состоит в образовании трехбромистого фосфора, который, реагируя с кислотой, дает ацилбромид. Последний гораздо легче подвергается енолизации по сравнению с исходной кислотой. Бром по видимому реагирует с енолом ацилбромида так же как с енолами кетонов.
2P + 3Br2
® 2PBr3
RCH2COOH
+ PBr3 ® RCH2COBr
+ POBr + HBr
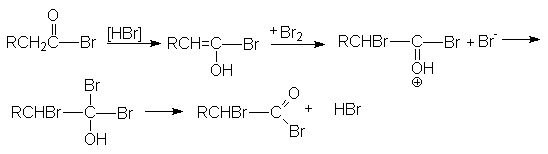
Регенерация исходного ацилбромида осуществляется за счет взаимодействия полученного монобромацилбромида с исходной кислотой.
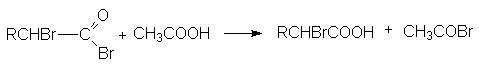
Хлор в присутствии следов фосфора реагирует аналогичным образом, но в целом менее селективно, поскольку конкурентно может происходить свободнорадикальное хлорирование во все положения углеродной цепи.
Взаимодействие с электрофильными реагентами
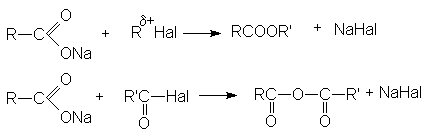
Атомы кислорода карбонильной группы недостаточно заряжены, чтобы быть объектом электрофильной атаки со стороны слабых и умеренных электрофильных реагентов. Для осуществления эффективной реакции электрофильного замещения по карбонильному углероду карбоксильной группы активируют, переводя ее карбоксилат – ионную форму. Тогда можно осуществить реакцию алкилирование, ацилирования и др.
Реакции восстановления карбоновых кислот
В целом карбоновые кислоты с трудом поддаются восстановлению как путем каталитического гидрирования, так и при действии натрия в спирте, но восстановление до первичных спиртов при действии литийалюминийгидрида или натрийборгидрида протекает достаточно энергично.
4RCOOH +
3LiAlH4 ® [(RCH2O)4Al]Li
+ 4H2 + 2LiAlO2
[(RCH2O)4Al]Li
+ 3H2O + HCl ® RCH2OH
+ Al(OH)3 + LiCl